أيض الكربوهيدرات Carbohydrate Metabolism
أ. هدم جلوكوز Glucose Oxidation
يشمل هدم جلوكوز الخطوات الآتية :
1. التحلل الجلايكولي Glycolysis (شكل 1 ): وفيه يتحطم جزيء جلوكوز ذي ذرات الكربون الست
إلى جزيئين من حامض بيروفيك pyruvic acid
(بيروفيت) كل منهما له ثلاث ذرات کربون، وتنطلق أثناء
ذلك طاقة حرة تسبب إنتاج جزيئين من ATP
كما يجري كذلك اختزال جزيئين من *NAD
إلي * NADH+ H يعطيان مزيدا من
الطاقة لاحقا عبر سلسلة نقل الإلكترون. يجدر بنا أن نلاحظ أن مقدار الطاقة الناتجة
من التحلل الجلايكولي هي صغيرة نسبيا إذ أنها تساوي حوالي 5 % من مجموع ATP الناتج من هدم جلوكوز ولذا فإن كمية الطاقة
هذه وحدها لا تكفي لأيض الخلايا كما أن معظم الخلايا لا تحوي تراكيز كافية من
أنزيمات التحلل الجلايكولي لكي تعتمد على هذا التحلل لاستخراج الطاقة الضرورية
لنشاطاتها الحيوية.
يستثنى من ذلك خلايا الدم الحمراء التي تعتمد بشكل
أساسي على التحلل الجلايكولي نظرا لعدم وجود ميتوكوندريا بها ، وخلايا العضلات
الهيكلية التي لديها كميات كافية من هذه الأنزيمات لكي تحصد محصولا مناسبة من
الطاقة بهذه الطريقة عندما تقل كمية أكسجين الواصلة إليها. ففي العضلات المخططة،
ونظرا لأن التحلل الجلايكولي لا يحتاج إلى أكسجين، أي يتم تحت ظروف لاهوائية، فإن
الخلايا تستفيد من التحلل الجلايكولي لإنتاج الطاقة التي تمكنها من الاستمرار في
الانقباض أثناء ظروف نقص أكسجين.
وتذهب الخلايا العضلية خطوة أبعد من ذلك بتحويلها حامض
بيروفيك وهو الناتج النهائي للتحلل الجلايكولي إلى حامض لبنيك lactic acid الذي يتراكم في العضلات ويرتبط تراكمه فيها
بالتعب fatigue لكن الخلية في
هذه الخطوة الأخيرة تحول بعضا من + NADH + H الذي نتج أثناء
التفاعلات السابقة إلى الشكل المؤكسد *NAD
والذي لا يستمر التحلل الجلايكولي بدون تواجده.
عند تحول حامض بيروفيك إلى حامض لبنيك في ظروف
لاهوائية، يعاد إنتاج مرافق الأنزيم لكي يستخدم ثانية في خطوة
التفاعل رقم 6 من تفاعلات تحلل جلوكوز.
في مرحلة لاحقة، أي بعد انتهاء التمرين الرياضي، يتحول
حامض لبنيك ثانية إلى حامض بيروفيك في الكبد وهذا يسلك بعد ذلك أكثر من طريق فقد
يكتمل تحطيمه إلى ثاني أكسيد الكربون والماء بدورة كربس، أو يتحول ثانية إلى جلوكوز
بعملية تدعى بناء جلوكوز جديد gluconeogenesis
بسبب كون معظم تفاعلات التحلل الجلايكولي قابلة للانعكاس، أي تتم باتجاهين، كما سنوضح
في فقرات لاحقة.
2. تكوين أستيل مرافق الأنزيم أ Formation
of acetyl coenzyme
A
يدخل حامض بيروفيك (والذي يكون عادة على هيئة أيون
بيروفيت pyruvate السالب) إلى
حشوة ميتوكوندريا من مكان تكونه في السيتوبلازم. هناك ترتبط مجموعة أستيل -CH3CO منه بمرافق الأنزيم
أفيكونان معا أستيل مرافق الأنزيم أ الذي يدخل إلى دورة کربس كما
سنبين لاحقا. يخرج أثناء هذه الخطوة جزي CO2
على هيئة غاز يطرد إلى الدم فالرئتين ويتكون جزيء واحد من + NADH + H مقابل كل جزيء بيروفيت يمر بهذه الخطوة
(تذكر أن جزيء جلوكوز واحد يعطي جزيئين من بيروفيت.
3. دورة كربسKrebs cycle ( دورة حامض الليمون citric acid cycle أو دورة الحوامض ثلاثية
الكربوكسيل( - trica(boxylic acid cycle (TCA
تتم هذه الدورة في حشوة ميتوكوندريا حيث يتحد أستيل
مرافق الأنزيم أ ثنائي الكربون) مع مركب رباعي الكربون هو حامض أوكسالو أستيك
ليكونان معا مركبا سداسي الكربون هو حامض الليمون citric acid
حيث يتحرر مرافق الأنزيم أليعيد الكرة مرة أخرى إذ يرتبط ثانية بأستيل وهكذا.
تكوين أستيل مرافق الأنزيم أمن حامض بيروفيك ومرافق
الأنزيم أ.
أما حامض الليمون فإنه يمر خلال سلسلة من التفاعلات
الأنزيمية منتجا أثناء ذلك مركبات ذات ثلاث مجموعات كربوكسيل. يتحرر بعد ذلك CO2
بالتدريج مما ينتج مركبات خماسية الكربون ثم رباعية الكربون ويكون آخر هذه المركبات
حامض أوكسالو أستيك الذي بدأت به الدورة والذي يعود ثانية للاتحاد مع أستيل مرافق
الأنزيم أجديد.
خلال هذه السلسلة من التفاعلات الأنزيمية ينتج جزي واحد
من ATP على هيئة GTP
أولا) من كل دورة وذلك بطريقة الفسفرة على مستوى المادة الحليلة كما يتكون ثلاث
جزئيات من * NADH + H
وجزيء واحد من FADH2 (وهذه مركبات مختزلة حاملة للإلكترونات
وقادرة على إطلاق الطاقة عند مرورها بسلسلة نقل الإلكترون). وحيث أن دورة كربس تتم
مرتين لكل جزيء جلوكوز ، فإن النواتج النهائية للدورة الجلوكوز واحد هي 2FADH2 ،
2ATP ، 6NADH إضافة إلى أربع جزئيات من CO2
.تجدر الإشارة إلى أن تفاعلات دورة كربس نفسها لا تحتاج إلى الأكسجين لإتمامها
ولكن أكسدة المرافقات الأنزيمية مثل: FADH2 ، NADH + H التي تتم أثناء سلسلة نقل الإلكترون، وتحديدا على الغشاء الداخلي
لميتوكوندريا ، تحتاج إلى الأكسجين كمستقبل نهائي للإلكترونات أثناء عملية
الأكسدة. فإذا لم تجر هذه الأكسدة فإن محتوى الخلية وميتوكوندريا من الصورة
المؤكسدة لهذه المركبات، FAD ، NAD
ينضب وبالتالي لا يمكن إتمام تفاعلات دورة كربس نفسها.
الخطوات التسع لتفاعلات دورة كربس
4. سلسلة نقل الإلكترون والفسفرة التأكسدية Electron transport
chain & oxidative Phosphorylation
بالإضافة إلى الطاقة التي نتجت من الفسفرة على مستوى
المادة الحليلة أثناء التحلل الجلايكولي ودورة كربس فإن بعض الطاقة لايزال كامنة
في المركبات المختزلة + FADH2 ، NADH + H ، التي نتجت في الخطوات
الثلاث السابقة. تعد هذه المركبات، بشكل عام، ذات طاقة اختزال وتأكسد كامنة سالبة
وهذا يجعلها أقل ألفة للإلكترونات، لهذا فإنها يمكن أن تتأكسد بأن تعطي
الإلكترونات لسلسلة من المركبات البروتينية من نوع سيتوكروم cytochrome
تدعى سلسلة نقل الإلكترون والتي تترتب بروتيناتها في ثلاث مجموعات بحيث أن أولاها
لديها ألفة أقل للالكترونات م ن الثانية وهذه لديها ألفة أقل من الثالثة أو
الأخيرة. هذا الترتيب يجعل الإلكترونات تنتقل أولا من * NADH + H مثلا إلى المركب البروتيني الأول وهذا
يعطيها بدوره للمركب الثاني الذي يعطيها للمركب الثالث. وحيث أن أكسجين ذو ألفة
أعلى للإلكترونات من هذه المركبات جميعا، فإن المركب الثالث يعطي الإلكترونات إلى
أكسجين الذي يشكل المستقبل النهائي للإلكترونات.
يمكن تلخيص سلسلة تفاعلات التأكسد والاختزال التي
وصفناها للتو على النحو التالي:
وحيث أنه Gک لهذا التفاعل
هي 53kcal / mol
- (أي أنه تفاعل منتج للطاقة) لذا فإن الطاقة الناتجة يمكن أن تستخدم في بناء ATP
بواقع.
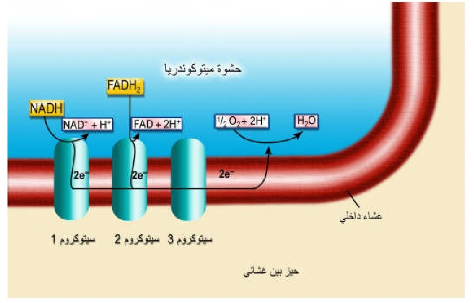
تنتقل الإلكترونات عبر سلسلة سيتوكروم الموجودة في
الغشاء الداخلي لميتوكوندريا. ويتزامن نقل الإلكترونات باتجاه الأكسجين مع أكسدة
المركبات الناقلة الوسيطة مثل NAD،
FAD .
7kcol لكل مول من ATP أي أنه نظريا
يمكن بناء حوالي 7 جزيئات من ATP ولكن ذلك غير
ممكن عمليا بسبب تبدد جزء من الطاقة على هيئة حرارة.
نظرية الكيميائية الأسموزية Chemiosmosis
ما الذي تستفيده الخلية من عمليات التأكسد والاختزال
التي وصفناها في الفقرة السابقة ؟ عندما تنتقل الإلكترونات من ناقل إلى آخر فإن
الطاقة المتحررة تستخدم لنقل أيونات هيدروجين*H
من حشوة ميتوكوندريا إلى الحيز بين غشائي ميتوكوندريا منتجة طاقة كيميائية كامنة
على هيئة فرق جهد كيميائي لأيونات هيدروجين عبر غشاء ميتوكوندريا الداخلي وبسبب
الربط بين فرق التركيز الكيميائي للهيدروجين وعمليات النقل المسببة له فقد أطلق
على هذه العملية الكيميائية الأسموزية chemiosmosis يمكن للطاقة
المتحررة من الإلكترونات المنطلقة من أن NADHتضخ أيونات
هيدروجين أكثر مما تضخه تلك المنطلقة من FADH2 الذي لا يعطي
إلكترونات إلا في مرحلة متأخرة نسبيا من سلسلة نقل الإلكترون. ماذا تصنع أيونات
هيدروجين المتواجدة بين غشائي ميتوكوندريا؟ هناك ثلاث مواقع على طول سلسلة نقل
الإلكترون يتواجد فيها مركبات بروتينية تشكل قنوات يمكن لأيونات هيدروجين أن تعبر
خلالها عائدة نحو حشوه ميتوكوندريا وفي كل موقع من هذه المواقع يمكن أن تنتقل
الطاقة الكامنة لتسبب إنتاج ATP من ADP +Pi بمساعدة الأنزيم مولد ATP synthase ATP))
وهكذا فإن NADH يمكن أن يحرر إلكترونات تسبب إنتاج ثلاث
جزيئات ATP بينما يحرر FADH2إلكترونات
تسبب إنتاج جزيئين من ATP.
تخليق ATP حسب الكيميائية الأسموزية. يضخ هيدروجين من حشوة ميتوكوندريا نحو الحيزبين الغشاءين حيث يتسرب ثانية حسب فرق التركيز الكهروكيميائي فيقوم مولد ATP بالاستفادة من طاقة التدفق هذه مولد ATP .
المحصول الإجمالي للطاقة الناتجة من تحطيم مول واحد من جلوكوز
ب. بناء جلوكوز Glucose synthesis
تحصل الخلية على جلوكوز بتحطيم جليكوجين، لكن بناء
جزيئات جديدة من جلوكوز من مصدر غير جليكوجين، وهي عملية تدعى توليد جلوكوز جديد gluconeogenesis
يتم أيضا في الخلية بالاستفادة من بيروفيت أو جلسرول أو من مشتقات الأحماض
الأمينية.
ففي الكبد والكلية تستطيع الخلايا أن تحول بيروفيت إلى
فسفواينول بيروفيت ( hosphoenolpyruvate( PEP)
أي عكس الخطوة العاشرة في التحلل الجلايكولي بواسطة سلسلة من التفاعلات داخل
ميتوكوندريا يضاف فيهاCO2 إلى بيروفيت ليتكون مركب رباعي الكربون هو
حامض أوكسالأستيك الذي يمكن أن يدخل دورة كربس أو أن يمر بخطوات أيضية ليخرج من
ميتوكوندريا إلى السيتوسول ويتحول إلى PEP.وحيث أن معظم
تفاعلات التحلل الجلايكولي المتبقية هي تفاعلات منعكسة فإن PEP
يتحول إلى جلوكوز .
وبعكس التحلل الجلايكولي الذي ينتج طاقة على شكل ATP،
فإن تحويل بيروفيت إلى جلوكوز يستهلك 6 مول من ATP
مقابل كل مول من جلوكوز ينتج. وحيث أن معظم الأنزيمات التي تشجع التحلل الجلايكولي
هي نفسها تشجع بناء جلوكوز جديد لذا فإن حاجة الخلية هي التي تقرر بأي اتجاه تسير
التفاعلات، فإذا كانت الخلية مثلا بحاجة إلى الطاقة فإن التفاعلات تسير باتجاه
التحلل الجلايكولي. يمكن للخلية كذلك أن تولد جلوكوز جديد من جلسرول الناتج من
تحلل ثلاثيات جلسرول ولكنها لا تستطيع بناءه من الأحماض الدهنية. كما يمكن للخلية
أن تولد جلوكوز جديد من الأحماض الأمينية بعد نزع مجموعة الأمين منها وتحويلها إلى
أحماض كيتو ketoacids حيث يمكن أن يتحول بعضها إلى بيروفيت، وهذا
يسلك مسار التحلل الجلايكولي باتجاه عكسي لبناء جلوكوز جديد.
التفاعلات الأيضية التي تؤدي إلى توليد جلوكوز جديد حيث
يمكن أن يبنى جلوكوز جديد من جليسرول ومن بيروفيت ومن حامض لبنيك ومن وسائط
الأحماض الأمينية.
ج. بناء جليكوجين Glycogen synthesis
لا يخزن الجسم سوى كميات قليلة من جلوكوز تكفي لإمداده
بالطاقة في الأوقات التي لا يكون فيها هناك امتصاص له من القناة الهضمية. أما باقي
جلوكوز الذي يصل إلى الجسم فإنه يخزن على هيئة جليكوجين في العضلات حوالي 600 غرام
) وفي الكبد ( والي 110غم).
آليات بناء جليكوجين من جلوكوز في الأنسجة المختلفة ومن
حامض بيروفيك الناتج من عملية تحلل جلوكوز.
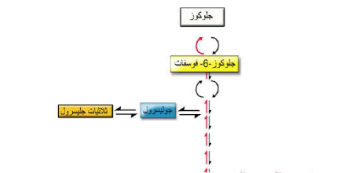
يمثل الشكل المسار الأيضي لبناء جليكوجين. فخلايا الجسم
جميعها تحول جلوكوز إلى جلوكوز. 6. فوسفات باستهلاك ATP
وهذا المركب يتحول، إذا تواجد بكمية أكبر من حاجة الخلية، إلى جليكوجين. يتم هذا
التحول عادة بتنظيم من هرمون انسولين insulin ويمكن إعادة
تحطيم جليكوجين (كما تشير الأسهم في الشكل ) لإعطاء جلوكوز . 6. فوسفات بتنظيم من هرمونات
جلوكاجون و إبينفرين وغيرها. ويمكن لمركب جلوكوز . 6. فوسفات الناتج من تحطم
جليكوجين أن يتحول ثانية إلى جلوكوز في خلايا الكبد حيث يمر إلى الدم ثم يصبح
متاحا للخلايا كوقود، أو أن يدخل في تفاعلات التحلل الجلايكولي منتجا بيروفيت كما
يحدث في خلايا العضلات وخلايا الجسم الأخرى.
الفصل الرابع:
·
دفق الطاقة في النظام الحيوي
الأرضي
·
العوامل المحددة لمعدل
التفاعلات الكيميائية
·
تفاعلات التأكسد والاختزال
في الخلية
المصادر
- التشريح الوظيفي وعلم وظائف الأعضاء ، الدكتور شتيوي العبدالله (2012) ، دار المسيرة عمان – الأردن.
- Prosser, C. Ladd (1991). Comparative Animal Physiology, Environmental and Metabolic Animal Physiology (4th ed.). Hoboken, NJ: Wiley-Liss. pp. 1–12. ISBN 978-0-471-85767-9.
- Hall, John (2011). Guyton and Hall textbook of medical physiology (12th ed.). Philadelphia, Pa.: Saunders/Elsevier. p. 3. ISBN 978-1-4160-4574-8.
- Widmaier, Eric P.; Raff, Hershel; Strang, Kevin T. (2016). Vander's Human Physiology Mechanisms of Body Function. New York, NY: McGraw-Hill Education. pp. 14–15. ISBN 978-1-259-29409-9.
- R. M. Brain. The Pulse of Modernism: Physiological Aesthetics in Fin-de-Siècle Europe. Seattle: University of Washington Press, 2015. 384 pp., [1].
- Rampling, M. W. (2016). "The history of the theory of the circulation of the blood". Clinical Hemorheology and Microcirculation. 64 (4): 541–549. doi:10.3233/CH-168031. ISSN 1875-8622. PMID 27791994. S2CID 3304540.
- Bernard, Claude (1865). An Introduction to the Study of Ex- perimental Medicine. New York: Dover Publications (published 1957).
- Bernard, Claude (1878). Lectures on the Phenomena of Life Common to Animals and Plants. Springfield: Thomas (published 1974).
- Brown Theodore M.; Fee Elizabeth (October 2002). "Walter Bradford Cannon: Pioneer Physiologist of Human Emotions". American Journal of Public Health. 92 (10): 1594–1595. doi:10.2105/ajph.92.10.1594. PMC 1447286.
- Heilbron, J. L. (2003). The Oxford Companion to the History of Modern Science, Oxford University Press, p. 649, link.
- Feder, ME; Bennett, AF; WW, Burggren; Huey, RB (1987). New directions in ecological physiology. New York: Cambridge University Press. ISBN 978-0-521-34938-3.
- Garland, Jr, Theodore; Carter, P. A. (1994). "Evolutionary physiology" (PDF). Annual Review of Physiology. 56 (1): 579–621. doi:10.1146/annurev.ph.56.030194.003051. PMID 8010752.










Comments
Post a Comment