الكمون الغشائي أو فرق جهد الراحة Membrane potential (Resting potential)
لقد بين نموذج الفسيفساء السائل أن غشاء الخلية يتكون
في هيكله الأساسي من طبقتين من الدهون المفسفرة التي تملك القليل من المجموعات
الوظيفية المشحونة charged كما أن هذه الدهون لا تسمح بمرور الشحنات
الكهربائية خلالها ولذا فإنها تشكل مقاومة ( resistance ( R
لمرور الأيونات أو التيار الكهربائي. كما بين النموذج أن هناك بروتينات عديدة
يخترق بعضها طبقتي الدهون و أن بعض هذه البروتينيات يمكن أن يشكل قنوات لمرور
الأيونات أولمرور التيار current ((I
. هكذا يبدو لنا أن غشاء العصبون بشكل عازلا ومقاومة لمرور التيار ويفصل بين سائلين
هما السائل داخل الخلايا المحتوى على كثير من أيونات بوتاسيوم وأيونات الجزيئات
العضوية كالبروتينات، والسائل خارج الخلايا المحتوى على عديد من أيونات صوديوم
وكلور.
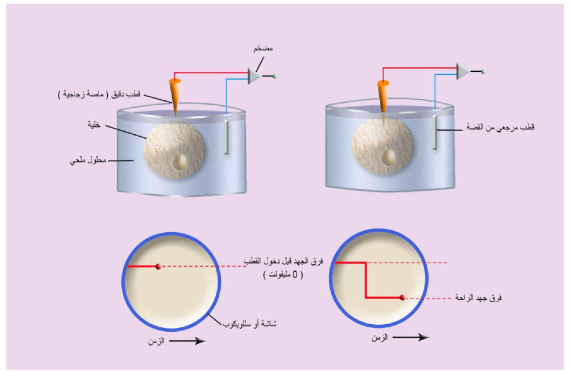
كيفية قياس الكمون الغشائي لخلية موضوعة في محلول ملحي:
قبل دخول الماصة الزجاجية داخل الخلية (إلى اليسار) ، وبعد دخولها إلى اليمين).
الرسم السفلي يبين قيمة فرق الجهد في الحالتين.
فإذا كانت الشحنات الموجودة على جانبي الغشاء غير
متماثلة فإنه يصبح لها القدرة potential على إنجاز شغل
إذا سمح لها بالتدفق نحو بعضها البعض. تدعى هذه القدرة بالجهد الكهربائي electrical
potential كما يمكن أن تدعى فرق الجهد potential
difference نظرا لاعتمادها على الفرق في تركيز الشحنات بين الجانبين، وغالبا
ما يستخدم علماء الفيزيولوجيا تعبير جهد potential ( V ; E)
لوحده للإشارة الفرق الجهد بين جانبي الغشاء وتستخدم وحدة فولت (Volt)
للإشارة إليه ولكن نظرا لأن فرق الجهد في معظم الأنظمة البيولوجية صغير جدا فإن
الدارج استخدام وحدة ميليفولت millivolt ( (mV .
يحكم قانون أوم العلاقة بين التيار (I)
وفرق الجهد (E) والمقاومة (R)
في الأنظمة البيولوجية كما هو الحال في الدوائر الكهربائية حيث
I =E/R
لقد وجد الباحثون أن جميع الخلايا الحية لها فرق جهد
أثناء الراحة يدعى فرق جهد الراحة resting potential ( (Er أو الكمون الغشائي membrane potential ( Em).
وقد جرى قياس فرق جهد الغشاء هذا باستخدام مقياس فرق جهد حساس voltmeter.
يتم القياس بوضع قطب موصل في السائل خارج الخلايا وآخر في السائل داخل الخلية (أي
يخترق غشاء الخلية)، ويضخم فرق الجهد بينهما بواسطة مضخم حيث يعرض على شاشة جهاز
أوسلوسكوب.
رسم يبين كيفية تدفق التيار نحو الداخل عند جعل الماصة
سالبة .
من الرواد في قياس الكمون الغشائي الباحثان C . Ling
و R . Gerard حيث استخدما عام 1949 ماصة زجاجية صغيرة ذات
قمة مدببة يمكن أن تدخل داخل الخلية دون إحداث ضرر كبير لها، وتعبأ الماصة بسائل
موصل (3M KC1 ) ويوضع فيها من جهتها الواسعة سلك من الفضة
يوصل بسلك آخر إلى قطب المضخم. أما القطب الآخر فقد كان سلكا آخر من الفضة موضوع
في السائل خارج الخلية وموصول إلى القطب الآخر للمضخم.
عندما تغمر الخلية بمحلول ملحي فيزيولوجي ويوضع القطبان
في هذا المحلول فإن مقياس فرق الجهد (أوسللوسكوب) سيشير إلى الصفر حيث أن السائل
الموصل بين القطبين هو المحلول الملحي الذي تتوزع فيه الشحنات بالتساوي ولذا لا
يوجد فرق في الجهد بين نقاطه المختلفة. عندما تدخل قمة الماصة الزجاجية داخل
الخلية فإن انحرافا نحو الأسفل في شعاع الإلكترونات الخاص بالأوسللوسكوب يظهر على
الشاشة معلنا أن الماصة الزجاجية قد اخترقت الغشاء وأن فرق الجهد عبر الغشاء
هوبمقدار الإنحراف الظاهر على شاشة الجهاز حيث يمكن تقديره بشكل دقيق إذ تجرى
معايرة الجهاز سلفا لمعرفة قيمة الانحراف. يعتمد مقدار جهد الراحة ( Er ،
Em
) على نوع الخلية التي يجري فحصها وهوعادة يتراوح في الخلايا الحية بين - 50 وحتى
- 100 مليفولت فهو خلايا الدم الحمراء - 9 وفي العصبونات بين - 40 وحتى - 75 وفي
العضلات الملساء. - 55 وفي العضلات المخططة - 80 وفي العضلات القلبية - 90 مليفولت
وقد جری اعتماد فرق جهد العصبون بأنه - 70 ملليفولتا.
أما الإشارة السالبة التي تسبق هذه الأرقام فتشير إلى زيادة الشحنات السالبة داخل الخلية
مقارنة بخارجها.
يمكن دراسة الخصائص الكهربائية لغشاء الخلية وفهم
التغيرات التي تحدث عبر هذا الغشاء بإضافة ماصة زجاجية دقيقة إلى الجهاز السابق حيث
تدخل الماصة داخل الخلية ويحقن بواسطتها نبضة من تيار كهربائي لكي يحدث اضطرابا في
فرق جهد الغشاء حيث يلاحظ الباحث سلوك الخلية إزاء هذا التنبيه أو الاضطراب. إذ
يمكن جعل التيار يتدفق نحو الداخل أي نحو السيتوبلازم أو جعله يتدفق نحو الخارج أي
خارجا من السيتوبلازم اعتمادا على اتجاه التيار الكهربائي المحقون بواسطة الماصة.
من المتعارف عليه أن تدفق التيار الأيوني يتم من منطقة
موجبة نسبيا إلى منطقة سالبة نسبيا وأن ذلك يكون مصحوبا بهجرة الشحنات (الأيونات
الموجبة بنفس هذا الاتجاه. بناء عليه فإنه عند جعل الماصة موجبة فإنها سترسل تیارا مباشرة
نحو السيتوبلازم وهذا يسبب تدفق التيار نحو الخارج outward current
عبر غشاء الخلية، كما أنه عند جعل الماصة سالبة فإن شحنات موجبة ستسحب من الخلية
مما يسمح بدخول تيار من السائل المحيط إلى السيتوبلازم ويسبب تدفق تيار نحو الداخل
inward
current .
الأساس الأيوني لفرق جهد الراحة Ionic basis of membrane potential
عند قولنا أن فرق جهد الراحة للعصبون هو - 70 مليفولت
فإن هذا يعني وجود زيادة في الشحنات السالبة داخل الخلية وزيادة في الشحنات
الموجبة خارج الخلية. تكون الشحنات المختلفة هذه منجذبة نحو بعضها البعض على جانبي
الغشاء المؤلف من الدهون العازلة كهربائيا وبذا فإن الغشاء يعمل كمكثف ( capacitor
( Ca . في الغالب تتراكم الشحنات الموجبة والسالبة
على جانبي الغشاء بينما يبقى معظم السائل داخل الخلية
ومعظم السائل خارج الخلية متعادلا كهربائيا. ويمكن معرفة الأساس الأيوني لفرق جهد
الراحة اعتمادا على عاملين هما الفرق في تركيز الأيونات بين داخل الخلية وخارجها
والفرق في نفاذية غشاء الخلية للأيونات المختلفة.
الفرق في تركيز الأيونات بين داخل الخلية
وخارجها
يمثل الجدول توزيع الأيونات الرئيسية عبر غشاء خلية
عصبية
توزيع الأيونات الرئيسية عبر غشاء خلية عصبية حركية
نخاعية في الثدييات
إن الجدول (7-1) لا يعني أن هذه هي الأيونات الوحيدة ف
ي العصبون إذ أنها تحتوي على 'SO4 ، HPO4 ،
HCO3
، H ، Mg ، Ca
وأحماض أمينية وبروتينات ولكن تركيز هذه الأيونات يقل بكثير عن تركيز الأيونات
الثلاث الرئيسية المبينة في الجدول بحيث يصبح تأثيرها على فرق جهد الغشاء قليلا.
إن المتتبع للجدول يلاحظ أن تركيز " Na خارج الخلية
أعلى بحوالي 10 مرات منه داخلها وهذا يعني أنه حسب قوانين الانتشار يجب أن يتوزع
صوديوم هذا بالتساوي خارج وداخل الغشاء إذا ما كان الغشاء منفذا له. بعبارة أخرى،
إن وجود فرق تركيز كيميائي chemical gradient لصوديوم يدفع بأيونات
صوديوم الموجبة لتعبر الغشاء ( أي يتدفق تيار صوديوم INa)
وهذا يجعل داخل الغشاء أقل سالبية مما كان عليه. بصورة مماثلة، فإنه يوجد فرق
تركيز كيميائي لبوتاسيوم يؤدي إلى حدوث تیار بوتاسيوم
Ik
يتدفق نحو الخارج مما يجعل داخل الخلية أكثر سالبية. وحيث أن فرق التركيز
لبوتاسيوم أكبر منه الصوديوم (حوالي 30 مرة مقابل 10 مرات) لذا فإن من المتوقع أن
يؤدي الفرق في التركيز الكيميائي هذا إلى دفع عدد أكبر من أيونات بوتاسيوم نحو
الخارج مقابل عدد أقل من أيونات صوديوم نحو الداخل.
ماذا سيكون أثر ذلك على فرق جهد غشاء الخلية؟ إن أخذ
هذا العامل لوحده بعين الاعتبار يؤدي إلى جعل داخل الخلية سالبة، وهكذا فلو بدأنا
بعصبون وكان فرق جهده بشكل افتراضي صفرا فإنه بمرور الوقت نتوقع أن يصبح داخله
سالبا بسبب خروج عدد أكبر من أيونات بوتاسيوم الموجبة نحو الخارج مقارنا بعدد
أيونات صوديوم الداخلة. يعرف نفاذ أيونات بوتاسيوم وصوديوم بسبب فرق التركيز بأنه
نفاذ عبر قنوات بوتاسيوم وصوديوم السلبية passive Na ' and K
" channels كما يعرف التيار الناتج عن مرورهما بأنه تيار
تسربي leak current .
الفصل السابع:
·
الكمون
الغشائي أو فرق جهد الراحة
·
الأساس الأيوني لفرق جهد
الراحة
·
الفرق في تركيز الأيونات بين
داخل الخلية وخارجها
·
التهيجية
·
الأساس الأيوني لسلوك الخلية
أثناء جهد الفعل
·
التغذية الراجعة الإيجابية
أثناء جهد الفعل
·
نقل جهد الفعل عبر العصبون
الواحد في الألياف اللاميلينية
·
غشاء العصبون كدائرة
كهربائية
·
استجابة الأعصاب الكاملة
للمنبهات
·
تقنية ربط الفولتية (ربط فرق
الجهد )
المصادر
- التشريح الوظيفي وعلم وظائف الأعضاء ، الدكتور شتيوي العبدالله (2012) ، دار المسيرة عمان – الأردن.
- Prosser, C. Ladd (1991). Comparative Animal Physiology, Environmental and Metabolic Animal Physiology (4th ed.). Hoboken, NJ: Wiley-Liss. pp. 1–12. ISBN 978-0-471-85767-9.
- Hall, John (2011). Guyton and Hall textbook of medical physiology (12th ed.). Philadelphia, Pa.: Saunders/Elsevier. p. 3. ISBN 978-1-4160-4574-8.
- Widmaier, Eric P.; Raff, Hershel; Strang, Kevin T. (2016). Vander's Human Physiology Mechanisms of Body Function. New York, NY: McGraw-Hill Education. pp. 14–15. ISBN 978-1-259-29409-9.
- R. M. Brain. The Pulse of Modernism: Physiological Aesthetics in Fin-de-Siècle Europe. Seattle: University of Washington Press, 2015. 384 pp., [1].
- Rampling, M. W. (2016). "The history of the theory of the circulation of the blood". Clinical Hemorheology and Microcirculation. 64 (4): 541–549. doi:10.3233/CH-168031. ISSN 1875-8622. PMID 27791994. S2CID 3304540.
- Bernard, Claude (1865). An Introduction to the Study of Ex- perimental Medicine. New York: Dover Publications (published 1957).
- Bernard, Claude (1878). Lectures on the Phenomena of Life Common to Animals and Plants. Springfield: Thomas (published 1974).
- Brown Theodore M.; Fee Elizabeth (October 2002). "Walter Bradford Cannon: Pioneer Physiologist of Human Emotions". American Journal of Public Health. 92 (10): 1594–1595. doi:10.2105/ajph.92.10.1594. PMC 1447286.
- Heilbron, J. L. (2003). The Oxford Companion to the History of Modern Science, Oxford University Press, p. 649, link.
- Feder, ME; Bennett, AF; WW, Burggren; Huey, RB (1987). New directions in ecological physiology. New York: Cambridge University Press. ISBN 978-0-521-34938-3.
- Garland, Jr, Theodore; Carter, P. A. (1994). "Evolutionary physiology" (PDF). Annual Review of Physiology. 56 (1): 579–621. doi:10.1146/annurev.ph.56.030194.003051. PMID 8010752.



Comments
Post a Comment