المولارية
Molarity
التركيز
الجزيئي الحجمي ) الجزيئية
الحجمية)
تعريف المولارية : المولارية هي عدد المولات المذابة في
لتر من المحلول.
صيغتها الرياضية :
حيث Vsol : هي حجم
المحلول باللتر.
دورق محدود السعة
ويمكن صياغة القانون السابق بالتعبير عن حجم المحلول
بالملتر أو السنتيمتر المكعب cm3 كما يلي :
وتكون وحدة المولارية هي مولار (molar)
وتختصر بالرمز (M) أو mol/ L (وبدون العلامة
(0) تكتب الوحدة mol / L كالتالي : (mol L-1)
ونظرا لأن L = 1 dm31 فإن وحدة
المولارية يمكن أن تكون : mol L-1 1 =mol dm31
ويمكن اشتقاق عدة قوانين كما يلي :
وتعتبر العلاقة الأخيرة من العلاقات الهامة في تحضير
محاليل ذات تراكيز معينة من المواد الصلبة
العلاقة
بين المولارية والنسبية المئوية الوزنية والكثافة المحلول
% Wt : النسبة
المئوية الوزنية
d: كثافة المحلول بوحدة (g/ml)
M : المولارية بوحدة mol /L
Mw: الوزن الجزيئي بوحدة (g/mol).
مثال/ ما مولارية محلول يحتوي على mol3
من سكر الجلوكوز (C6H12O6)
مذاب في كمية من الماء بحيث يصبح حجم المحلول ml750؟
الحل
مثال / محلول مائي حجمه cm200
يحتوي على g2 من هيدروكسيد الصوديوم (NaOH)
احسب المولارية لهذا المحلول الأوزان الذرية : (23 =H = 1 , 0 = 16 ,
Na).
مثال / احسب مولارية محلول كلوريد الصوديوم في الماء إذا
أذيب منه (mol 0.735) في كمية من الماء بحيث يصبح حجم المحلول
(ml650).
بتطبيق العلاقة :
شاهد ايضاً :
·
المول
·
تعريف
المحلول - صور المادة المذابة في المحلول - أنواع المحاليل السائلة
·
تطبيقات على النسبة المئوية
الوزنية
·
الكسر
المولي (الكسر الجزيئي)
·
المولالية
(التركيز الجزيئي الوزني)
·
المولارية
(التركيز الجزيئي الحجمي)
·
العلاقة بين المولارية
والنسبة المئوية الوزنية والكثافة لمحلول
·
التخفيف
·
النسبة المئوية الوزنية
والكسر المولي للمادة النقية
المصادر
·
أحمد عبد العزير العويس
و سليمان حماد الخويطر و عبد العزيز إبراهيم الواصل و عبد العزيز عبد الله السحيباني
، الكيمياء العامة ، دار الخريجي، الرياض، 1996م.
·
جوردن م بارو، الكيمياء
الفيزيائية، ترجمة أحمد محمد عزام، دار ماجروهيل، 1998م.
·
سليمان حماد الخويطر
و عبد العزيز عبد الله السحيباني، الثرموديناميك الكيميائي، دار الخريجي، الرياض، 1998م.
·
سمير مصطفى المدني،
أساسيات الكيمياء العامة، جامعة الملك سعود - النشر العلمي و المطابع، الرياض، 1998م.
·
الكيمياء العامة -
احمد بن عبدالعزيز العويس و آخرون- دار الخريجي للنشر و التوزيع ط2. 1996م.
·
سمير مصطفى المدني
، كتاب أساسيات الكيمياء العامة ، ( منشورات جامعة الملك سعود1997
م.
·
حسن محمد الحازمي و
محمد إبراهيم الحسن ، كتاب الكيمياء العضوية ، مكتبة الخريجي
1990م.
·
Ralph H. Petruccii and William S.
Harwood, General Chemistry, Principle and Modern Applications, Prentice-Hall,
New Gersey, 1997.
·
James E. Brady and John R. Holum,
Chemistry, The study of Matter and its Changes, Wiley, New York, 1993.
·
Petter Atkins and Loretta Jones,
Chemistry, Matter and Change, 3d Edition, W.H. Freedman and Co., New York,
1997.
·
James E. Brady, General Chemistry,
Principles and Structure, 5th Edition, Wiley, New York, 1990.
·
David E. Goldberg, Schaum's
Outline Series, Theory and Problems of Chemistry Foundations, International
Editions, McGraw-Hill, New York, 1991.
·
James E. Brady and John R. Holum,
Fundamentals of Chemistry, 34 Edition, Wiley, New York, 1988.
·
Raymond Chang, Chemistry, 5th
Edition, International Edition, McGraw-Hill, New York, 1994.
·
R. Abu-Etta, Y. Essa and A.
El-Ansary, General Chemistry, Cairo University Press, 1998.
·
P.W. Atkins, Physical Chemistry,
Oxford Press, Oxford, UK, 1982.
·
G.M. Barrow. Physical Chemistry,
MacGraw-Hill, New York, USA, 1996.
·
Maurice Wahba, Hanna A. Rizk, Introduction
to Physical Chemistry, Anglo Egyptian, 1978.
·
Robert A. Alberty and Robert J.
Silby, Physical Chemistry, Wiley, New York, 1992.
·
Whitten, etal , General Chemistry
with Qualitative Analysis , 3rd ed., Saunders college publishing



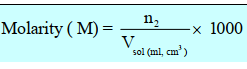
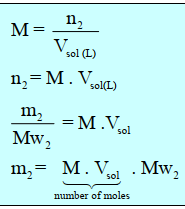
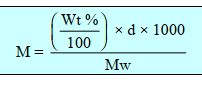



Comments
Post a Comment